-
Produkte
-
Laborgeräte
-
Labor-Messgeräte und Elektroden
Kalibrierstandards
- Chemikalien, Reagenzien und Standards
-
Online-Analysatoren
Chlor-Analysatoren Chlordioxid Phosphat-Analysatoren
- NP6000sc
- FX610/FX620 System
- Filtrax System
- Phosphax sc
- Phosphax sc LR
- 5500 sc
- NP6000sc Chemistry/Reagents
- Phosphax Sigma
Analysatoren der EZ-Serie- Eisen
- Aluminium
- Mangan
- Phosphat
- Chlorid
- Cyanid
- Fluorid
- Sulfat
- Sulfid
- Arsen
- Chrom
- Kupfer
- Nickel
- Zink
- Ammonium
- Gesamt-Stickstoff
- Gesamt-Phosphor
- Phenol
- Flüchtige Fettsäuren
- Alkalinität
- ATP
- Härte
- Toxizität
- Probenvorbereitung
- Bor
- Farbe
- Nitrat
- Nitrit
- Kieselsäure
- Wasserstoffperoxid
- EZ Serie Reagenzien
- Anorganische Stoffe – EZ sc-Serie
- EZ Series Zubehör
- EZ sc Series Additional Analyzers
- Metalle – EZ sc-Serie
- Nährstoffe – EZ sc-Serie
-
Online-Sensoren und Controller
Digitale Controller (Transmitter) Controller (analog)
- SC4500
- Orbisphere 366x Ex
- Orbisphere 410/510 Kohlendioxid
- Orbisphere 410/510 Ozon
- Orbisphere 410/510 Sauerstoff
- Orbisphere 51x Wasserstoff
- 3400 Analoge Kontakt-LF
- 3400 Digitale Kontakt-LF
- 3700 Analoge induktive LF
- 3700 Digitale induktive LF
- 3798 sc Elektrodenfrei
- 9525 DCCP System
pH- und Redox-Sonden- 12 mm pH/Redox
- 1200-S Redox
- 1200-S pH
- 8362 sc Reinstwasser
- Differential pH
- Digital Differential Redox
- Digital Differential pH
- Kombination pH/Redox
- LCP Redox
- LCP pH
- Automatisierte Laborsysteme
- Multiparameter Online Panels
- Claros Water Intelligence System
- Probenehmer
-
Laborgeräte und Verbrauchsmaterial
Instrumente Allgemeines LaborverbrauchsmaterialGeräteGlas-/KunststoffprodukteLiteratur und Referenzmaterial
- Testkits und Streifen
-
Mikrobiologie
Gebrauchsfertige Nährmedien
- BART Tests
- Flüssiges MPN
- Gesamtkeimzahl Nährmedien
- Hefe und Schimmelpilze
- MUG Röhrchen
- Membran-Filtration
- P/A (An-/Abwesenheit)
- Paddle Testers
Laborbedarf- Flaschen, Röhrchen, Küvetten und Gestelle
- Mikrobiologie Filter
- Petrischalen & Zubehör
- Probensammelbeutel
- Trichter, Pumpen und Anschlüsse
- Zubehör
Trockennährmedien Zubehör und Chemikalien - Elektrochemie
-
Laborgeräte
- Parameter
-
Softwarelösungen
-
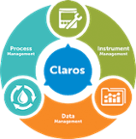
Claros Water Intelligence System
Produktsäulen Process Management
- Lösungen für:
- BSB-/CSB-Entfernung
- Nitrifikation/Denitrifikation
- Phosphorelimination
- Schlammbehandlung
Data Management- Lösungen für:
- Erfassung
- Visualisierung & Analyse
- Berichterstattung
- Datengenauigkeit
Instrument Management- Lösungen für:
- Wartung
- Fehlerbehebung
- Fernzugriff
- Labor- und Prozessvergleich
Branchenheraus-
forderungen Einhaltung gesetzlicher Vorschriften Kosteneinsparungen Fernbetrieb Data Management Prozessoptimierung Gerätewartung
-
Claros Water Intelligence System
- Branchen
- Unterstützung
- News
Switzerland
Wählen Sie Ihr Land oder Ihre Region aus:
Europe
Americas
Asia - Australasia
- Australia
- Mainland China
- India
- Indonesia
- Japan
- Malaysia
- New Zealand
- Philippines
- Singapore
- South Korea
- Thailand (Thai)
- Taiwan
- Vietnam
Middle East - Africa
Chlor
Was ist Chlor?
Chlor ist ein chemisches Element mit der Ordnungszahl 17 und einer Atommasse von 35,5. Es kommt in der Natur in gebundener Form, z.B. als Natriumchlorid (Kochsalz) vor. Chlor wird kommerziell durch Elektrolyse aus Natriumchloridlösung hergestellt.
Freies Chlor
Bei Verwendung zur Desinfektion bildet sich freies Chlor, wenn Chlorgas in Wasser gelöst wird. Je nach pH-Wert können sich zwei chemische Stoffe bilden (beide sind starke Desinfektionsmittel):
- Hypochlorige Säure (HOCl)
- Hypochlorit-Ionen (OCl -).
Chlorung
'Bei der Chlorung handelt es sich um einen Wasseraufbereitungs- und Desinfektionsprozess, bei dem freies Chlor verwendet wird. Die Chlorung ist die übliche Desinfektionsmethode für Rohwasser mit minimaler organischer Kontamination und geringen Konzentrationen schwer zu behandelnder Mikroorganismen wie Giardien oder Cryptosporidium. Sie wird auch zur Geschmacks- und Geruchskontrolle, zur Verhinderung von Algenwachstum, zur Erhaltung klarer Filtermedien, zur Entfernung von Eisen und Mangan, zum Abbau von Schwefelwasserstoff und Cyanid sowie zur Verbesserung der Koagulation verwendet.
Chloramin (gebundenes Chlor)
Chloramine bilden sich, wenn dem ammoniakhaltigen Wasser Chlor zugegeben wird. Eine Reaktion von Chlor mit Ammoniak kann erwünscht oder unerwünscht sein, je nach Wasseraufbereitungsstrategie. Je nachdem, wie viele Wasserstoffatome in den Ammoniummolekülen durch Chloratome ersetzt werden, können sich drei verschiedene Chloraminformen bilden:
- Monochloramin
- Dichloramin
- Trichloramin
Chloraminierung
Bei der Chloraminierung handelt es sich um einen Wasseraufbereitungs- und Desinfektionsprozess, bei dem Monochloramin als Ziel-Desinfektionsmittel verwendet wird. Chloramine weisen im Vergleich zu freiem Chlor eine geringere Reaktivität auf und reagieren weniger intensiv mit verschiedenen Verunreinigungen im Rohwasser, insbesondere mit organischen Substanzen. Dadurch entstehen weniger krebserregende Desinfektionsnebenprodukte (DNP), hauptsächlich Trihalomethane (THM). Dies ist einer der wichtigsten Gründe für die Forderung, die freie Chlorung durch Chloraminierung zu ersetzen.
Zudem besteht bei Chloraminen aufgrund der geringeren Oxidationsleistung ein deutlich geringerer Desinfektionsmittelbedarf. Dadurch wird weniger Chlor benötigt, um den gewünschten Gesamtchlorgehalt im Wasser zu erhalten, wodurch wiederum weniger Aufbereitungskosten anfallen.
Gesamtchlor
Gesamtchlor ist die Summe aller in der Probe vorhandenen Formen von freiem und gebundenem Chlor. Es gibt spezielle Methoden zur Messung von freiem Chlor (hypochlorige Säure und Hypochlorit) und gebundenem Chlor (Chloramine und chlororganische Verbindungen).
Warum sollte man Chlor messen?
Als starkes Oxidationsmittel eignet sich Chlor (Cl 2) ideal als Desinfektionsmittel. Durch angemessene Restchlorwerte im Trinkwasser wird sichergestellt, dass das Wasser für den menschlichen Verzehr unbedenklich ist. Zu viel Chlor im Wasser kann jedoch negative Auswirkungen auf die pharmazeutische Produktion, Membranbehandlungsprozesse und andere Anwendungen haben. Überschüssiges Restchlor kann sich schädlich auf die Umwelt auswirken und die organoleptischen Eigenschaften von Leitungswasser beeinträchtigen.
Wird Wasser mit Chlor versetzt, findet eine Reaktion unter Bildung von freiem Chlor oder Chloraminen (bei Vorhandensein von Ammoniak) statt. Diese:
- fungieren als starke Germizide.
- oxidieren Metalle, sodass sie entfernt werden können.
- lindern unangenehmen Geschmack und Gerüche.
Bei Hach® finden Sie die Test-Kits, Geräte, Reagenzien, Schulungen und Software zum Thema Chlor, die Sie für die Überwachung und Verwaltung des Chlorgehalts in Ihrer spezifischen Anwendung benötigen.
Empfohlene Produkte zur Chlorüberwachung
Wählen Sie aus zahlreichen Optionen den passenden Hach Desinfektionsanalysator für Ihre spezifischen Anwendungen aus.
Weitere InformationenDie benutzerfreundlichen, robusten und tragbaren Messgeräte von Hach sind für die besonderen Belastungen vor Ort ausgelegt.
Weitere InformationenSeit über 70 Jahren ist Hach im Bereich der Spektralphotometrie innovativ und bietet viele der führenden Spektralphotometer auf dem Markt für Wasseranalytik an.
Weitere InformationenSL1000 – PPA: portabler Parallel-Analysator – tragbares Colorimeter mit USB
Der SL1000 portable Parallel-Analysator (PPA) von Hach führt Messungen mit weniger als der Hälfte der manuellen Arbeitsschritte durch.
Weitere InformationenReagenzien für freies und Gesamtchlor
Hach hat es sich zum Ziel gesetzt, hochwertige Reagenzien für routinemäßige und anspruchsvolle Wasseranalysen bereitzustellen.
Weitere Informationen
Die Chemie hinter den Strategien der Chlordesinfektion
Der Chlorbedarf ist die Gesamtmenge an Chlor, die für eine Reaktion mit allen Verunreinigungen im Wasser wie Metallen, Bakterien, organischen Substanzen oder Ammoniak erforderlich ist. Wenn freies Chlor zugesetzt wird und mit den Verunreinigungen reagiert, wird es aufgebraucht. Wird dabei der Bedarf überschritten, ist freies Chlor messbar. Der Chlorbedarf ist daher die Differenz zwischen der dem Wasser zugefügten Chlormenge und der messbaren Restchlormenge, die nach der Reaktion verbleibt.
Das Verständnis des Chlorbedarfs trägt zur Gewährleistung einer effektiven Desinfektion während des gesamten Wasseraufbereitungsprozesses bei. Bei der Breakpoint-Chlorung wird eine ausreichende Menge an Chlor eingesetzt, um eine Restmenge an freiem Chlor zu erhalten.
Risiken im Zusammenhang mit der unsachgemäßen Handhabung von Restchlor
- Gesundheit - Wasser, das für die Dialyse verwendet wird, muss von Chlor gereinigt werden, um Patienten vor weiteren gesundheitlichen Problemen zu schützen.
- Umwelt - Selbst in geringen Konzentrationen kann Chlor Umweltschäden verursachen. Dies gilt insbesondere für in Wasser und Boden lebende Organismen.
- Bauwesen - Chloride, die sich durch die Verwendung von gechlortem Wasser bilden können, verursachen möglicherweise Spannungsrisse im Edelstahl und können so Anlagen und Strukturen beschädigen.
- Pharmazeutika - Chlor kann sich schädlich auf aktive pharmazeutische Wirkstoffe während der Produktion auswirken, was zu einer schlechten Produktqualität und Produktverlust führen kann.
- Wasseraufbereitungsanlagen - In Wasseraufbereitungssystemen kann Chlor Umkehrosmosemembranen und Ionenaustauscherharze beschädigen.
Entchlorungsmethoden
Da Chlor schädlich sein kann, gibt es Anwendungen, die eine „Entchlorung“ erfordern. Bei der Adsorptionsentchlorung wird Aktivkohle verwendet, um Chlorverbindungen zu entfernen. Bei der chemischen Entchlorung werden Reduktionsmittel wie Sulfite, Bisulfite oder Metabisulfite verwendet, um bestimmte Formen von Chlor zu zerstören.
Für welche Prozesse ist eine Chlorüberwachung erforderlich?
Trinkwasseraufbereitung und -verteilung
Während der Voroxidation wird Rohwasser, das in die Anlange gelangt, mit Chlor versetzt (Vorchlorung), um in einer primären Aufbereitungsstufe (außer Desinfektion) Mineralien auszufällen. So wird die Entfernung von suspendierten und gelösten Substanzen vor der Filtration unterstützt. Das Wasser wird dann gefiltert, um die Klarheit zu verbessern, und anschließend wieder gechlort.
Damit das Chlor wirksam ist, muss die Konzentration vor und nach der Filtration (neben pH-Wert, Wassertemperatur und Kontaktzeit) überwacht und kontrolliert werden. Wasserwerke verfügen über ein Absetzbecken, in das Chlor injiziert, gemischt und je nach Temperatur, pH-Wert und Art der im Wasser vorhandenen Mikroorganismen für die entsprechende Zeit mit dem Wasser in Kontakt gehalten wird. Durch die Kontaktzeit entsteht eine Restchlormenge, die dafür sorgt, dass das Wasser beim Eintritt in die Lagerbecken und beim Durchlaufen des Verteilungssystems sauber bleibt.
Die gesamte Chlorung vor (Vorchlorung) und nach Filtern (Nachchlorung) wird während des gesamten Aufbereitungsprozesses und im Verteilungssystem an mehreren Punkten kontrolliert. Zusätzliche Booster-Chlorung von Leitungswasser im Netz wird in der Regel an Pumpen-/Booster-Stationen durchgeführt und muss sorgfältig überwacht und kontrolliert werden.
Die Überwachung der Chlorkonzentration im Verteilungssystem ist von entscheidender Bedeutung, da so sichergestellt wird, dass die richtige Menge an Restchlor eingehalten wird, um die vorgeschriebenen Desinfektionsstandards zu erfüllen, und dass keine übermäßige Chlormenge vorhanden ist.
Vorteile der Verwendung von Chlor zur Desinfektion von Trinkwasser
- Chlor beseitigt Schleimbakterien, Schimmelpilze und Algen, die üblicherweise in Wasserreservoirs, an den Wänden von Wasserleitungen und in Lagertanks wachsen.
- Chlor ist ein starkes Germizid, das die Konzentration vieler krankheitsverursachender Mikroorganismen im Trinkwasser auf ein regulatorisch zulässiges Maß reduziert.
- Chlor entfernt gelöstes Eisen und Mangan aus dem Rohwasser.
- Chlor reduziert unangenehmen Geschmack und Gerüche durch:
- Oxidation natürlicher organischer Substanzen wie faul riechender Algensekrete, Sulfide und Gerüche durch faulende Vegetation.
- Abbau von Schwefelwasserstoff, der einen Geruch nach faulen Eiern hat.
- Entfernung von Ammoniak und anderen stickstoffhaltigen Verbindungen, die einen unangenehmen Geschmack verursachen können.
Nachteile der Verwendung von Chlor zur Desinfektion von Trinkwasser
- Chlor ist nicht gegen Cryptosporidium, einen lebensbedrohlichen Parasiten, wirksam.
- Während der Chlorung kann unerwünschtes Ammoniak mit Chlor unter Bildung von Chloraminen reagieren, die das Desinfektionspotenzial verringern und bei nicht effizienter Überwachung und Kontrolle zu Geschmacks-/Geruchsproblemen führen können.
- Bei der Reaktion mit organischen Substanzen im Wasser kann Chlor Desinfektionsnebenprodukte (DNP) bilden, die als gesundheitsschädlich gelten. Aufgrund dieser Risiken gibt es Vorschriften, die die DNP-Werte sowie die Restchlorkonzentrationen im Trinkwasser begrenzen.

Abwasseraufbereitung
Die Chlorung wird in den letzten Reinigungsstufen zur Abtötung von Pathogenen sowie von in früheren Aufbereitungsstufen verwendeten Mikroorganismen zur Verhinderung der Ausbreitung von durch Wasser übertragenen Krankheiten eingesetzt. Um die Toxizität des Abwassers zu verringern, wird die Entchlorung zur Kontrolle von Chlorrückständen und zur Einhaltung von Vorschriften eingesetzt, bevor Abwasser in die Vorfluter abgegeben wird. Chlor dient zur Oxidation von Cyaniden, die auf Chlorung ansprechen.

Industrielle Kühltürme
Der Chlorgehalt muss überwacht und kontrolliert werden, da bei zu niedrigen Chlorkonzentrationen das Biowachstum die Wassersysteme beeinträchtigen kann. Wenn der Chlorgehalt jedoch zu hoch ist, kann es zu Korrosion oder anderen Schäden kommen.

Lebensmittelverarbeitung
Chlor wird als Desinfektionsmittel für Obst, Gemüse, Geflügel und Fleisch verwendet. Die Aufrechterhaltung eines angemessenen Restchlorgehalts ist für die Optimierung der Desinfektionsleistung von Spülwasser von entscheidender Bedeutung. Im zirkulierenden Wasser, das für das Spülbad während der Pasteurisierung am Ende des Verpackungsprozesses verwendet wird, sammeln sich Verunreinigungen an. Daher ist es notwendig, einen Restchlorgehalt sicherzustellen, um eine Desinfektion des Wassers zu gewährleisten.

Clean-in-Place-Verfahren (CIP) in der Lebensmittel-, Getränke- und Pharmaindustrie
Rohrleitungen und Apparate, die in industriellen Prozessen eingesetzt werden, werden regelmäßig im Rahmen eines sogenannten „Clean-in-Place“-Verfahrens (CIP) gereinigt und desinfiziert. Chlor muss überwacht werden, um eine geeignete Konzentration zur Desinfektion in der CIP-Lösung sicherzustellen und eine Kontamination der Produkte aufgrund von zu wenig oder zu viel Chlor zu vermeiden.

Wie wird Chlor überwacht?

Colorimetrie
Im Allgemeinen kommen bei dieser optischen Methode Farbintensitätsmessungen zum Einsatz, um die Chlorkonzentration in einer Lösung zu bestimmen. Wenn der Probe entsprechende Puffer- und Indikatorlösungen hinzugefügt werden, erfolgt eine Reaktion unter Bildung einer Farbe, deren Intensität proportional zur Chlorkonzentration ist. Die Farbintensität wird mit dem Auge, dem Colorimeter oder dem Spektralphotometer gemessen. Diese Methode ist anfällig für Interferenzen durch Farbe und Trübung der Probe sowie durch einige chemische Substanzen neben Chlor, die gleichzeitig mit dem Indikator reagieren.
DPD-Methode
Die DPD-Methode ist die am häufigsten verwendete colorimetrische Methode zur Messung von Chlor. Sie kann zur Messung von freiem Chlor und Gesamtchlor mit Geräten vor Ort und im Labor sowie mit Online-Geräten verwendet werden. Die DPD-Methode kann jedoch durch andere Oxidationsmittel wie Mangan, Chrom und Chloramine beeinträchtigt werden.
Indophenol-Methode
Die Indophenol-Methode (selektiv auf Monochloramin) kann zur Messung von Monochloramin und freiem Ammoniak sowie freiem Chlor verwendet werden. Monochloramin wird direkt gemessen. Bei der Messung von Monochloramin und freiem Ammoniak mit derselben Probenmethode wird ein zusätzliches Reagenz verwendet, um freies Ammoniak in Monochloramin umzuwandeln. Freies Chlor kann auch mit der Indophenol-Methode unter Verwendung eines Systems mit zwei Reagenzien gemessen werden, das nicht den gleichen Interferenzen wie die DPD-Methode unterliegt. Diese Methode ist jedoch nur bei Laboranalysen und Analysen vor Ort anwendbar und nicht bei Online-Analysatoren.

Titration
Mit dieser Methode wird die Chlorkonzentration auf der Grundlage der chemischen Reaktion zwischen Chlor und dem zur Probe hinzugefügten Titranten bestimmt. Der Titrant wird schrittweise zugegeben, bis die Reaktion abgeschlossen ist. Der Endpunkt (oder Äquivalenzpunkt) ist der Punkt, an dem Titrant und Chlor ausgeglichen sind. Der Äquivalenzpunkt kann visuell mit einem Farbindikator oder mit einem elektrochemischen Sensor bestimmt werden. Manuelle, visuelle Messungen sind weniger präzise und anfälliger für Interferenzen durch Farbe oder Trübung der Probe. Die Titration mit Elektroden ist hingegen genauer und nicht für diese Interferenzen anfällig.
DPD-FEAS-Methode
Bei der DPD-FEAS-Methode wird ein magentafarbener visueller Indikator verwendet, der bis zu einem farblosen Endpunkt titriert wird. Diese Methode dient zur Messung von freiem Chlor und Gesamtchlor.
Iodometrische Methode
Bei der iodometrischen Methode wird ein blauer visueller Indikator verwendet, der am Titrationsendpunkt entfärbt wird. Diese Methode wird in der Regel zur Messung hoher Konzentrationen von Gesamtchlor verwendet.
Amperometrisch
Bei dieser Methode kommt die amperometrische Titration zur manuellen oder automatischen Bestimmung des Endpunkts zum Einsatz. An der Elektrode wird eine kleine Spannung angelegt, und der Endpunkt wird durch eine Stromänderung bestimmt, die sich aus der Reduktion von Chlor durch den Titranten (Phenylarsinoxid) ergibt. Die Änderung des Stroms und das Volumen des Titranten werden gemessen, um die Chlorkonzentration zu ermitteln. Diese Methode bietet Verfahren zur Messung von freiem und Gesamtchlor, Chlordioxid und Chlorit mithilfe von Titration und Rücktitration.

Online-Amperometrie
Bei dieser elektrochemischen Methode wird die Änderung des elektrischen Stroms gemessen, die sich aus den chemischen Reaktionen an den Elektroden ergibt, wobei der Strom proportional zur Chlorkonzentration ist. Es sind verschiedene amperometrische Sensordesigns verfügbar, die eine bessere Selektivität für verschiedene Chlorformen bieten. Diese Methode ist nicht anfällig für Beeinträchtigungen durch Farbe oder Trübung der Probe. Die Sensoroberfläche, die mit der Probe in Berührung kommt, ist jedoch anfällig für Verschmutzung. Einige amperometrische Analysatoren benötigen keine Reagenzien. Amperometrische Sensoren müssen gewartet und vor Ort mit einer Frequenz kalibriert werden, die von der Anwendung abhängt.
FAQ
Was ist Monochloramin und wie wird es bei der Wasserdesinfektion eingesetzt?
Monochloramin ist ein Desinfektionsmittel, das häufig als Alternative zu freiem Chlor zur Desinfektion von Trinkwasser verwendet wird, hauptsächlich weil beim Einsatz von Monochloramin weniger DNP entstehen als bei freiem Chlor.
Der Begriff Chloramine beschreibt in der Wasserindustrie die drei wichtigsten Verbindungen, die sich durch Reaktion von Ammoniak mit Chlor bilden lassen: Monochloramin, Dichloramin und Trichloramin. Monochloramin ist das Ziel-Desinfektionsmittel. Andere unerwünschte Verbindungen können im Wasser nachgewiesen werden, wenn die Chloraminierung nicht ausreichend kontrolliert wird, aber auch in chlorierten Grundwassersystemen, die natürliches Ammoniak enthalten, und in chlorierten Abwasserabläufen. Es ist wichtig zu beachten, dass sich Chloramine auf eine Gruppe von Verbindungen und nicht auf eine einzelne Substanz beziehen. Eine technische Beschreibung für diese Gruppe wäre „anorganische Chloramine“, um sie von den organischen Chloraminen zu unterscheiden, die eine geringe oder gar keine Desinfektionsleistung bieten. Grundsätzlich bilden sich die Chloramine der Reihe nach, z.B. zuerst Monochloramin, dann Dichloramin und schließlich Trichloramin, wenn das ammoniakhaltige Wasser kontinuierlich mit Chlor versetzt wird. Der Prozess verläuft jedoch umgekehrt, wenn chloriertem Wasser Ammoniak zugesetzt wird. Der Chloraminierungsprozess ist sehr komplex und erfordert für eine effiziente Steuerung wesentlich mehr Überwachung.
Das Ziel der Chloraminierung ist die vollständige Bildung von Monochloramin unter Vermeidung anderer Chloramine. Ein Cl 2 : N-Massenverhältnis von 5 : 1 hat sich als optimales chemisches Chemikalienzufuhrverhältnis herausgestellt, bei dem die Dichloraminbildung (Geschmacks- und Geruchsprobleme) verhindert, die Menge an nicht umgesetztem Ammoniak minimiert und die Biofilmbildung und Nitrifikation nachgelagert kontrolliert wird.
Was würde bei Verwendung von DPD zu positiven Ergebnissen führen, wenn in der Probe kein Chlor vorhanden ist?
Andere Oxidationsmittel wie Brom, Iod, Ozon, Chlordioxid, einige Metalle oder Wasserstoffperoxid können mit DPD unter verschiedenen Umständen reagieren und falsche positive Messwerte verursachen. Die häufigste Interferenz entsteht durch oxidiertes Mangan, was sich durch eine Behandlung der Probe mit Kaliumiodid und Natriumarsenit korrigieren lässt. Sonnenlicht kann während der 3-minütigen Reaktionszeit für Gesamtchlor mit dem DPD-Indikator reagieren (halten Sie die Probe während der Reaktionszeit bedeckt, wenn Sie im Freien messen).
Bei Chlorkonzentrationen im niedrigen Bereich kann gelöster Sauerstoff insbesondere bei direkter Sonneneinstrahlung Beeinträchtigungen verursachen. Wenn die ULR-Methode (ultraniedriger Messbereich) auf einem Colorimeter oder Spektralphotometer verwendet wird, stellen Sie sicher, dass ein Reagenzienblindwert mit entionisiertem Wasser ermittelt und von den Ergebnissen der Probenanalyse subtrahiert wurde. Es empfiehlt sich auch, dieselbe Probenküvette zum Nullen des Geräts und zum Ablesen der Probenkonzentration zu verwenden. Dadurch werden Effekte vermieden, die nur auf optische Unterschiede zwischen der Null- und der Mess-Küvette zurückzuführen sind.
In welchen Fällen wird das Indophenol-Reagenz für freies Chlor statt dem DPD-Reagenz für freies Chlor empfohlen?
Es gibt mehrere Gründe, die Indophenol-Methode für freies Chlor, die in der Hach Methode 10241 zum Einsatz kommt, der DPD-Methode vorzuziehen:
- Bestimmung der Restmengen an freiem Chlor in Gegenwart von Mangan und anderen Oxidationsmitteln, die colorimetrische DPD-Methoden und sowohl DPD- als auch amperometrische Titrationsmethoden für freies Chlor beeinträchtigen. Verwendung in Trinkwasser, gechlortem Trinkwasser, Schwimmbadwasser und aufbereitetem Abwasser.
- Bestimmung von freiem Chlor in Gegenwart von Chloraminen (freies Chlor sollte in der Wasserprobe prävalent sein). Chloramine reagieren mit dem DPD-Indikator für freies Chlor. Durch ihr Vorhandensein wird die entwickelte Farbe instabil, und es lässt sich eine langsame Zunahme im Laufe der Zeit verzeichnen. Die Interferenzrate hängt von der Konzentration von Chloraminen, deren Struktur, dem pH-Wert und der Temperatur der Probe ab. Daher ist es schwierig, den Grad der Interferenz anhand der tatsächlichen Menge an freiem Chlor vorherzusagen.
Bei der Indophenol-Methode für freies Chlor wird das in der Probe vorhandene freie Chlor mithilfe von Freechlor F Reagenzlösung schnell in Monochloramin umgewandelt. Das gebildete Monochloramin wird dann mit Monochlor F Reagenz bestimmt, das spezifisch für Monochloramin ist. Mangan, andere Chloramine und chlorierte organische Amine reagieren nicht mit dem Monochlor F Reagenz, sodass es nicht zu einer Beeinträchtigung bei der Bestimmung des freien Chlors kommt. Ein Monochlor F Probenblindwert wird verwendet, um in der Originalprobe vorhandene Monochloramine zu kompensieren.
Wann sollte der Gesamtchlorgehalt gemessen werden?
Der Gesamtchlorgehalt wird normalerweise in Systemen gemessen, bei denen die Chloraminierung zum Einsatz kommt, wenn eine beabsichtigte Reaktion von Chlor mit Ammoniak stattfindet. Als Gesamtchlor bezeichnet man die Summe aus freiem Chlor und anorganischen Chloraminen. Wenn die Chlorwerte einer Aufsichtsbehörde gemeldet werden müssen, sollte zunächst ermittelt werden, welche Form von Chlor (freies oder Gesamtchlor) gemessen und welche Methode für die Analyse verwendet werden soll.
Wann sollte der Gehalt an freiem Chlor gemessen werden?
Freies Chlor wird in Trinkwassersystemen gemessen, bei denen Chlorgas oder Natriumhypochlorit zur Desinfektion verwendet wird, um festzustellen, ob das Wasser ausreichend Desinfektionsmittel enthält. Typische Restchlorwerte in Trinkwasser liegen bei 0,2 - 2,0 mg/L Cl 2, wobei die Konzentrationen an der Eintrittsstelle (point of entry, POE) bis zu 4,0 mg/L betragen können. Wenn die Chlorwerte einer Aufsichtsbehörde gemeldet werden müssen, sollte zunächst ermittelt werden, welche Form von Chlor (freies oder Gesamtchlor) gemessen und welche Methode für die Analyse verwendet werden soll.